Desarrollado en colaboración con el Instituto Nacional de Técnica Aeroespacial (INTA) y publicado en la revista especializada ‘Proceedings of the National Academy of Sciences (PNAS)’, este trabajo revela que esta exploración adopta también una estructura fractal. Además, señala que distintos ambientes pueden impulsar la divergencia entre poblaciones virales.
«En lugar de moverse por el espacio genético como un caminante que avanza paso a paso, los virus exploran simultáneamente una gran nube de variantes», ha explicado la investigadora del Museo Nacional de Ciencias Naturales (MNCN) y del Centro Nacional de Biotecnología (CNB), Susanna Manrubia. Ambas entidades pertenecen al CSIC.
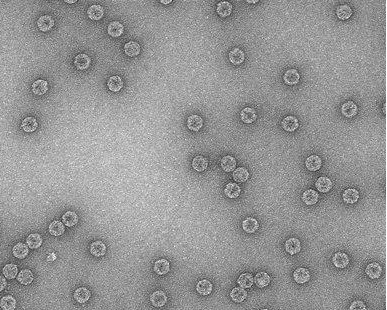
Para llegar a esta conclusión, la investigación se ha focalizado en el estudio del bacteriófago QB, que es un virus que infecta bacterias, cuyo genoma, al igual que el de otros virus que afectan a la salud humana y animal -como el SARS CoV 2, el virus de la polio y el virus de la fiebre aftosa-, está formado por una molécula de ARN que muta con gran rapidez.
Así, analizando millones de secuencias poblacionales del bacteriófago QB obtenidas mediante secuenciación profunda, se han reconstruido redes de genotipos que permiten visualizar la diversidad de variantes presentes en una población viral con un nivel de detalle sin precedentes. Con ello, se ha obtenido nueva información sobre la dinámica evolutiva de los virus de ARN, caracterizados por su velocidad para adaptarse a nuevos ambientes, y sobre los mecanismos moleculares que generan innovación biológica.
«Nuestro trabajo muestra que esta exploración tiene una organización jerárquica que genera un fractal, y que es masiva: unas pocas secuencias muy abundantes generan toda la diversidad genética posible a distancias cortas, junto con una periferia extensa de mutantes cada vez más raros», ha continuado Manrubia.
En este sentido, el estudio se refiere a la hipótesis clásica de exploración, que está protagonizada por la acumulación de mutaciones neutras, que alteran el genoma, pero no la estructura física del virus. Ello permitiría progresar con mutaciones silenciosas pero seguras que, a una escala de tiempo mucho mayor, finalmente sí generarían cambios más profundos.
COMPLEJAS REDES DE GENOTIPOS
«Frente a esta hipótesis, nuestros resultados indican que las poblaciones virales forman complejas redes de genotipos», ha destacado, no obstante, el investigador del CNB y del Instituto de Biología Evolutiva (IBE) del CSIC y de la Universitat Pompeu Fabra de Barcelona (UPF), Luís F. Seoane, quien ha añadido que, «en esas redes, las variantes más abundantes ocupan posiciones centrales desde las que generan mutantes cercanos en cascada, independientemente de que estos tengan mayor o menor viabilidad biológica».
A su juicio, «la exploración es tan masiva que los mutantes menos viables no afectan al conjunto de la población». «Sin embargo, sí funcionan como atajos, acelerando cambios que requerirían caminos evolutivos más largos con solo mutaciones neutras», ha declarado.
«Las poblaciones que evolucionan en circunstancias distintas empiezan a ocupar zonas diferentes de la red genética», ha manifestado, por su parte, la investigadora del Centro de Astrobiología (CAB) del CSIC y del INTA, Ester Lázaro, que ha estudiado también el comportamiento de poblaciones virales a diferentes temperaturas. Ello «sugiere que la especialización ecológica puede surgir de manera natural a medida que los virus exploran el espacio de mutaciones», ha afirmado.